По данным Всемирной организации здравоохранения, в 2012 году в Европе, СНГ, Прибалтике, Турции и Израиле на смерти от рака приходится около 22% всех смертей. Больше смертей приходится только на смерти от сердечно-сосудистых заболеваний. Эта страшная статистика широко известна.
По этой причине тема онкологических заболеваний — одна из самых горячих в науке. Онкологические заболевания изучают клеточные биологи, генетики, молекулярные биологи, биоинформатики и даже экологи. Абитуриенты, студенты биологических и медицинских факультетов, а также некоторые великие ученые по-прежнему мечтают найти «лекарство от рака». The game is on.
Ученые уже включили бензопилу CRISPR/Cas9, и анализируют ДНК опухолей. Мир замер в ожидании. То тут, то там возникают новые препараты. Тем обиднее за Оливера Сакса, известного нейробиолога и популяризатора науки, не дожившего трех месяцев до регистрации эффективного лекарства от одного из агрессивных видов рака, неоперабельной или метастазирующей меланомы.
Дьявол в мелочах
Исследовать ДНК разных видов злокачественных образований можно на разных этапах профилактики или лечения болезни. Представим здорового человека, который заботится о своем здоровье и знает историю своей семьи. Этого человека беспокоит, что его дед по материнской линии умер от рака прямой кишки, а у его матери подозрение на рак поджелудочной железы. При этом его отец здоров. Нашему герою интересно, кто внес основной вклад в генетический материал, связанный с работой его пищеварительной системы, и как ему планировать свою жизнь в долгосрочной перспективе.
Если на этом этапе наш герой сделает специальный анализ ДНК, в лаборатории изучат определенные участки его генома и сравнят их с типичными. Возможно несколько вариантов развития событий. У человека могут не обнаружить мутаций в локусах, ассоциированных с болезнью, найти ассоциированные с патологией или безопасные мутации. Ассоциация с патологией означает, что в мировых генетических базах данных зарегистрировано определенное число статистически значимых случаев заболевания определенным видом рака при наличии аналогичной мутации. Онкологические заболевания относят к мультифакториальным: обычно их развитие обусловлено мутациями в нескольких разных генах. Однако в определенных видах рака существуют особые гены, предопределяющие исход болезни более чем в половине случаев. Избежать ложноположительных или ложноотрицательных результатов нельзя. Так как во все сложные биологические процессы, к которым относится и канцерогенез, почти всегда вовлечен не один ген, а несколько, результат анализа, то есть вывод о предрасположенности к заболеванию, носит вероятностный характер.
Отбор локусов ДНК для анализа — отдельная большая задача, нужно тщательно выбрать локусы, достоверно ассоциированные с заболеванием. В целом, существует довольно много исследований по анализу ассоциаций между мутациями и заболеваниями, однако нередко найденные ассоциации ложноположительные. Это связано с тем, что были исследованы в основном геномы людей европеоидной расы. Это серьезно затрудняет возможность сделать персонализированную медицину доступной для всех в ближайшее время.
В общем, пессимистичный прогноз, полученный по результатам генетического анализа на мутации не следует воспринимать как приговор, а как мотивацию для пересмотра собственного образа жизни. Однако нужно обязательно проходить регулярные обследования для выявления возможных патологий и сообщать о результатах анализа врачу. Впрочем, обследования необходимы и тем, у кого не были обнаружены онкогенные мутации.
Внимание к женской груди
Для примера рассмотрим рак молочной железы. Так, девушкам и женщинам, близкие родственницы которых болели раком молочной железы, обязательно к прохождению генетическое исследование генов BRCA1 и BRCA2. Пациенткам с недавно диагностированным раком молочной железы это также показано для выбора лечения. Женщинам от 40 и старше необходимо пройти обследование (а также каждый год делать маммографию).
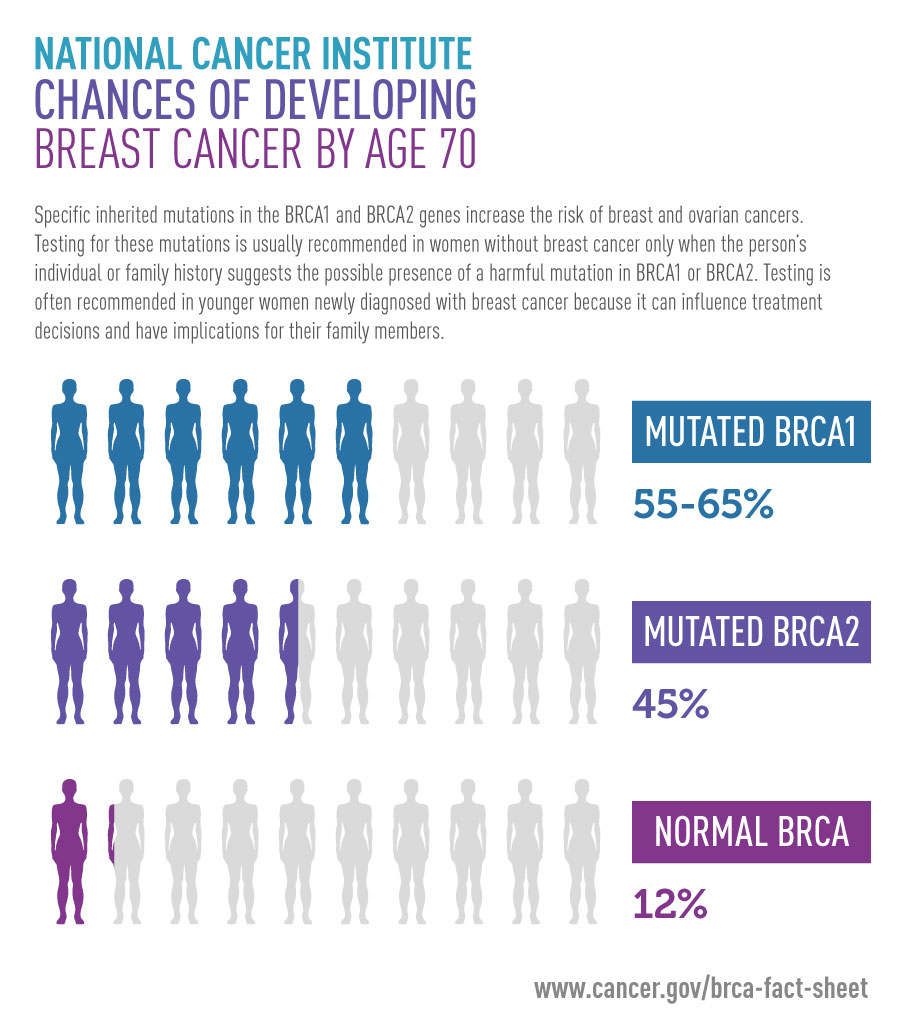
Немного молекулярной биологии, чтобы понять, что именно происходит, когда в гене есть мутация. Для примера возьмем знакомый BRCA1 (сокращение от «breast cancer»). Исходно это ген-супрессор опухоли, который синтезирует белок, отвечающий за починку ДНК («репарацию»). Если исправить ДНК невозможно, то гены BRCA1 подключают другие белки. Так запускается процесс клеточной смерти, и клетка с поломанной ДНК уничтожается. Как это работает: у женщины есть две копии гена BRCA1 — одна от мамы, одна от папы. Даже если у женщины есть только одна функционирующая копия гена BRCA1, белок вырабатывается. Он исправляет ДНК при нарушениях. Если поломаны обе копии гена, то BRCA1 перестает нормально функционировать и чинить ДНК. В таком случае риск рака груди очень высок.
Смотрите глубже
Теперь, возможна ситуация, когда у человека рак не был диагностирован. По сути, у него в ткани какого-то органа появилась клетка, которая развивается не по той же программе, что и остальные. При этом она не воспринимается собственными иммунными клетками как патология и продолжает активно делиться. С одной стороны, это непонятное образование мешает нормальной работе органа. С другой — оно обрастает кровеносными сосудами, специально стимулируя их рост, и забирает ресурсы здоровых тканей.
В начале этого года вышла статья о том, что раковую опухоль можно воспринимать как отдельную экосистему внутри собственного тела. Ученые предлагают новый подход к лечению рака: концепцию «экологической терапии». Суть заключается в том, что организм представлен как экосистема, а клетки, взаимодействующие между собой и с раковой опухолью — как отдельные виды. Основное отличие от традиционного видения противоопухолевой терапии — воздействие на все элементы «экосистемы», а не только применение «оружия» по отношению к раковым клеткам.
Множить сущности по необходимости
Если по-честному, то называть раком и лимфому, и саркому не совсем правильно. Происходят действительно похожие вещи: появляется группа клеток, отличающихся от окружения, которые при самом неблагоприятном стечении обстоятельств начинают мигрировать и захватывать новые органы. Исходно рак (карцинома) — злокачественное новообразование эпителиальной ткани, выстилающей внутренние полости органов. В иной плоскости лежит онкогематология — заболевания, связанные с клетками крови и лимфы.
В Genotek исследуется предрасположенность к 33 онкологическим заболеваниям. Вероятность каждого из заболеваний оценивается на основании определенного маркера или группы маркеров, подтвержденных на основании нескольких публикаций. На самом деле, исследовательские группы, занимающиеся раком, тоже классифицируют случаи заболеваний особым способом. Если говорить откровенно, то и эффективные лекарства от некоторых видов рака уже изобрели: меланома, лимфома Ходжкина, саркомя мягких тканей и другие. Впрочем, их использование на территории России пока недоступно.
Катарсис против рака
Рак лечат несколькими способами, тут приведено описание двух наиболее распространенных способов в самом общем виде. Из традиционных видов наиболее предпочтительным является оперативное лечение. Если опухоль операбельная и состояние пациента позволяет, то его отправляют к хирургу. В противном случае проводится химиотерапия — в пациента через катетер заливают коктейль из цитостатиков — веществ, которые препятствуют клеточному делению. Логика тут такая: если человек уже сформирован, то у самых важных органов нет активного роста клеток, а опухоль растет, пока клетки делятся. Если мы ограничим способность клеток делиться, то сможем убить опухоль.
Неприятными последствиями химиотерапии являются явления, связанные как раз с потребностью в делении клеток — выпадение волос, отмирание ворсинок кишечника, повреждение кожи и потеря фертильности у мужчин. Существуют и другие виды традиционного лечения, но при обзоре возникает неизгладимое впечатление, что даже при сохранении жизни противораковая терапия существенно ухудшает ее качество. По этой причине мы бы хотели сосредоточиться на лекарствах нового поколения.
Круглосуточная доставка яда
Иммунотерапия — инновационный подход к лечению рака. Идея в основе очень проста: действовать против рака методами иммунной системы. Нужно мобилизовать собственную или синтезировать ее подобие, чтобы доставлять те же яды адресно, а не пускать по всему кровотоку. Тогда нужно: (1) взять некий белок с поверхности опухолевой клетки, (2) синтезировать антитело, которое способно его распознать, и (3) связать это антитело с сильным ядом, который бы высвобождался при взаимодействии белка и антитела. Это позволило бы уменьшить циркуляцию отравляющего вещества в крови, с одной стороны, и увеличить ее в микроокружении опухоли, с другой. Прорывы в противоопухолевой терапии таких фармацевтических гигантов как Merck, Bayer или Sanofi, связаны с разработкой лекарств против отдельных заболеваний.
Back to the DNA
ДНК-тестирование позволяет исследовать генетические маркеры — узнавать последовательности генов, которые ассоциированы с теми или иными видами онкологических заболеваний. Зная, в каком участке гена находится поломка, можно понять, что повреждено. Более того, это помогает при подборе конкретного лекарства. Не нужно проводить биопсию — забор живой ткани, сравнимый по тяжести с операцией. В будущем, где победила персонализированная высокотехнологичная медицина, человеку будет достаточно сдать биологический образец на анализ и, при подтверждении неблагоприятного диагноза, получить персональное лекарство, сделанное по шаблону: антитело на белок клеток опухоли, связанное с лекарством; и вылечиться.
Финальная ремарка для читателей из России. Это — а не описание статистики — самая грустная часть. На территории нашего государства сильно ограничены возможности использования противоопухолевой иммунотерапии. По возможности, постарайтесь регулярно проходить обследование, ограничить себя и близких от стресса и вести здоровый образ жизни. Онкология на ранних стадиях легко оперируется и поддается лечению, поэтому своевременное выявление рисков и профилактика так важны. Всего вам доброго и с наступающими праздниками. Ваш Genotek.
Автор: Genotek






