Вторую часть своей эпопеи о предсказании биологической активности я хотел, на самом деле, посвятить совсем другим вещам. Однако у аудитории появились вопросы, и надо отвечать за базар.
Под биологической активностью понимается эффект, производимый веществом в организме. Этот аспект называется фармакодинамическим. Противоположный ему аспект, фармакокинетический, подразумевает воздействие организма на лекарство: его всасывание, распределение, метаболизм, выведение. Вся эта тетрада носит название ADME.
Казалось бы, какой интерес может представлять то, что организм делает с лекарством? А вот какой. Фармакокинетика даёт прогноз концентрации лекарства в тканевом пространстве организма через то или иное время после приёма. Это важно, так как от концентрации лекарства в органе-мишени зависит биологический ответ, который, напомню, может быть как терапевтическим, так и токсическим.
Концентрация вещества в организме понижается из-за его выделения (с потом и другими менее приятными биологическими субстанциями), так и по причине метаболизма – превращения его под действием ферментов в другие вещества. Продукты превращения, метаболиты, также могут обладать биологической активностью, причём не всегда благоприятной.
При желании метаболизм тоже можно рассматривать как проявление биологической активности – возможность подвергаться воздействию со стороны ферментной системы организма.
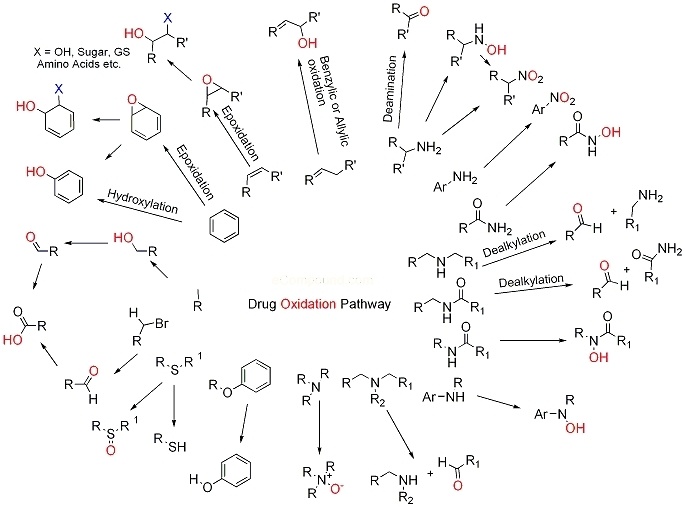
Задача метаболизма – обезвредить ксенобиотик (чужеродный для жизни объект). Большинство низкомолекулярных органических веществ не может быть превращено в стандартные отходы жизнедеятельности (воду, углекислый газ, мочевину и т.д.), поэтому обезвреживание зачастую сводится к 2 процессам, протекающим соответственно в 1-ую и 2-ую его фазы. На первом этапе (фаза модификации) молекула видоизменяется таким образом, что в ней появляются определённые функциональные группы – спиртовая, аминогруппа, карбоксильная, эпоксидный фрагмент и т.п. На втором этапе (фаза конъюгации) посредством этих групп происходит связывание первичных метаболитов с остатками, которые превращают всю конструкцию в водорастворимую, способную покинуть организм через почки. Чаще всего навешиваются остатки глюкуроновой, серной кислот, глицина, уксусной кислоты, глутатиона и т.п. Обратите внимание на то, что повышение гидрофильности таких конъюгатов достигается как увеличением числа водородных связей, так и возможностью ионизации.
Аудитория задала вопросы, как можно предсказать образование тех или иных метаболитов.
Отвечаю. Метаболизм 1-ой фазы протекает в основном в печени (хотя и во многих других органах тоже) под действием окислительно-восстановительных ферментов (оксидоредуктаз) и гидролитических ферментов (гидролаз), последние расщепляют сложноэфирные и амидные связи. Учитывая, что:
а) окислению подвергаются места молекулы с повышенной электронной плотностью, восстановлению – с пониженной;
б) гидролизу подвергаются сложноэфирные и амидные связи;
в) в результате 1-ой фазы должны получиться метаболиты с характерными функциональными группами, их предсказание сводится к предсказанию реакционной способности органического соединения по его структурной формуле – традиционной задаче для химиков-органиков.
Итак, внимание, смертельный эксперимент.
Открываю 12-ого Машковского на произвольной странице и тыкаю в первое попавшееся соединение. Страница 123, ацефен. Упс, в статье указаны метаболиты, так неинтересно. Попытка № 2. С 284. Суматриптан. Отлично, средство против мигрени. Работаем.
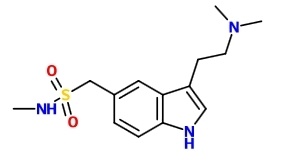
Видим, с «правого» конца третичную аминогруппу, которую было бы неплохо превратить в первичную, способную к конъюгации. С левого конца видим метилсульфонамид. Его надо деметилировать, опять обнажить первичную аминогруппу (в составе сульфонамидной группировки). Всё это происходит в организме путём окисления метилов в гидроксиметилы с последующим отлётом формильных фрагментов. Посередине имеем индол. Достаточно ароматичен, к электрофильной атаке сравнительно устойчив. Вспоминаем, что индол и скатол – естественные «ароматизаторы» биологических отходов, так что метаболизмом индольной системы можно пренебречь (раз она сохраняется в отходах).
Теперь гуглим «sumatriptan metabolism» и проверяем себя по статье.
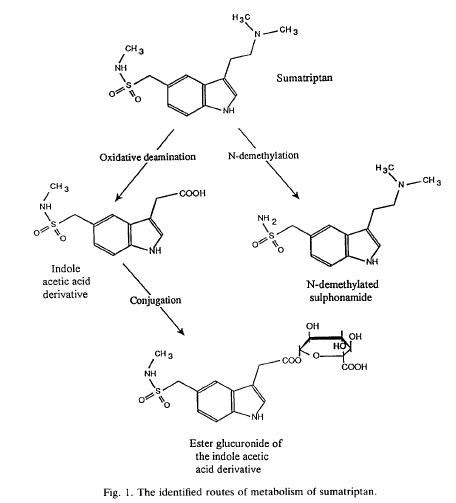
Деметилирование левой половины молекулы предсказано хорошо. С правой стороной похуже, хотя направление взято верное. Просто образованием первичного амина дело не заканчивается, окисление идёт более глубоко с образованием индолилуксусной кислоты.
Я честно тыкал наугад в Машковского ещё пар раз (стр. 396 – нитросорбид, метаболиты указаны в статье, стр. 411 – феникаберан, но не было возможности себя проверить, так как только 1 русскоязычная статья по фармакокинетике и та без метаболитов), пока не понял, что достаточно будет и 1 примера.
Меня спрашивали о том, зачем нужны программы для предсказания метаболизма, если всё и так хорошо предсказывается без них.
Во-первых, при большом количестве соединений в библиотеке анализ становится очень трудоёмким. Во-вторых, программы дают более полную информацию о подвергающихся изменению местах молекулы. Чтобы в этом убедиться, привожу скрины доступной он-лайн системы MetaPrint2D (http://www-metaprint2d.ch.cam.ac.uk/metaprint2d), которые вы можете сравнить с моими предсказаниями и с результатами эксперимента, приведёнными выше.
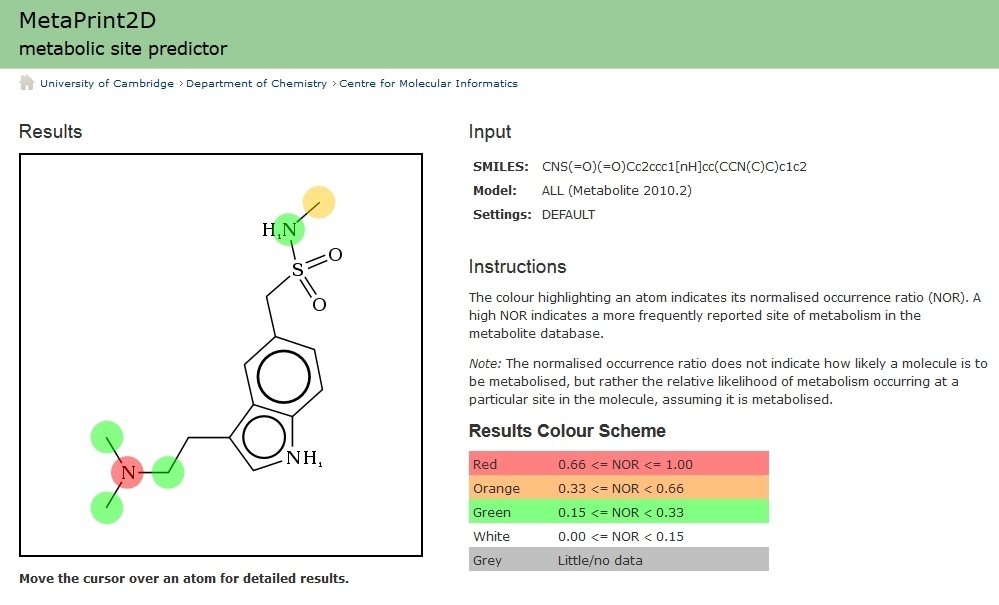
Обратите внимание также на формулировку NOR: этот параметр показывает, не с какой вероятностью будет метаболизироваться молекула, а относительную вероятность модификации того или иного её положения, при условии, что она происходит.
Для сравнения приведу ещё своё описание метаболизма феникаберана и результаты предсказания сайтов метаболизма другой доступной он-лайн программы.
Описание.
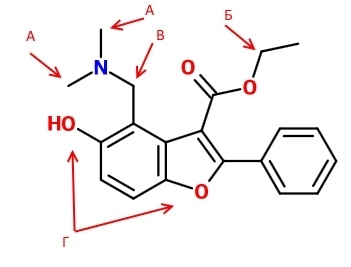
Гидролиз сложного эфира (Б), окислительное деметилирование третичного амина (А) с возможным более глубоким окислением до карбоновой кислоты (В), так как бензильное положение активировано к электрофильной атаке. Окисление конденсированного бензофурана с образованием хиноидной структуры (Г).
Как видите, я упустил возможность окисления фенила (в спешке из-за невнимательности, гидроксилирование пара-положения для меня очевидно), а программа SMARTCyp (http://www.farma.ku.dk/smartcyp/) не согласилась с возможностью образования хиноидной структуры, хотя, скорее всего, она просто не заточена под выдачу таких результатов.
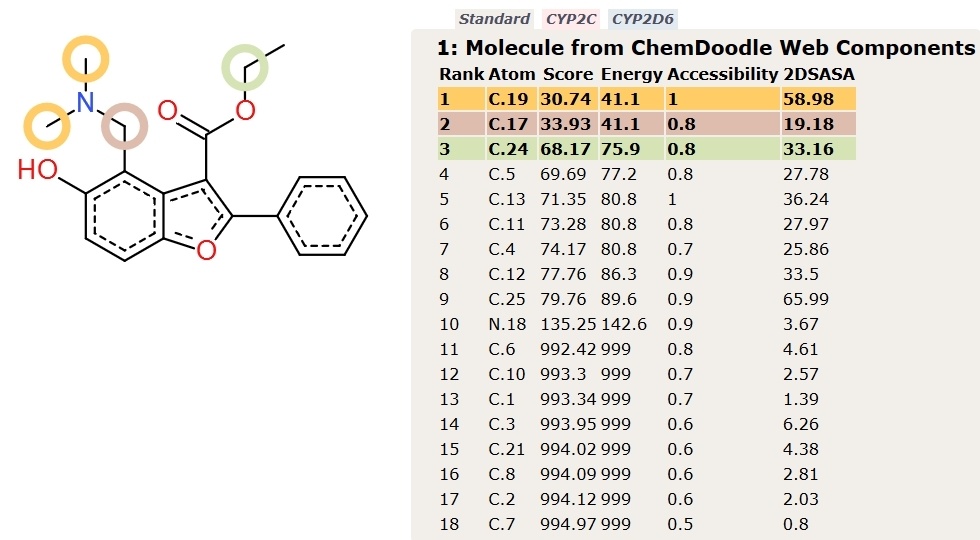
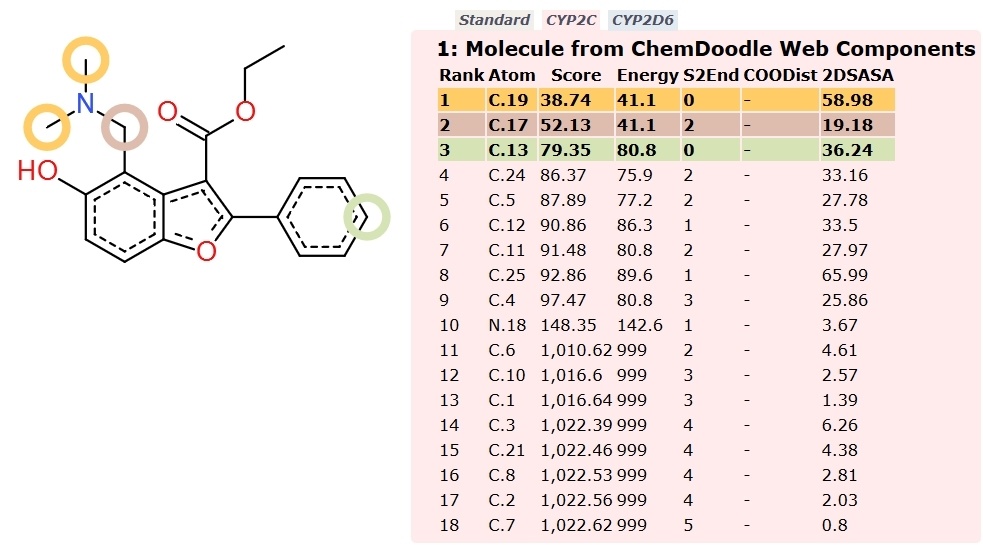
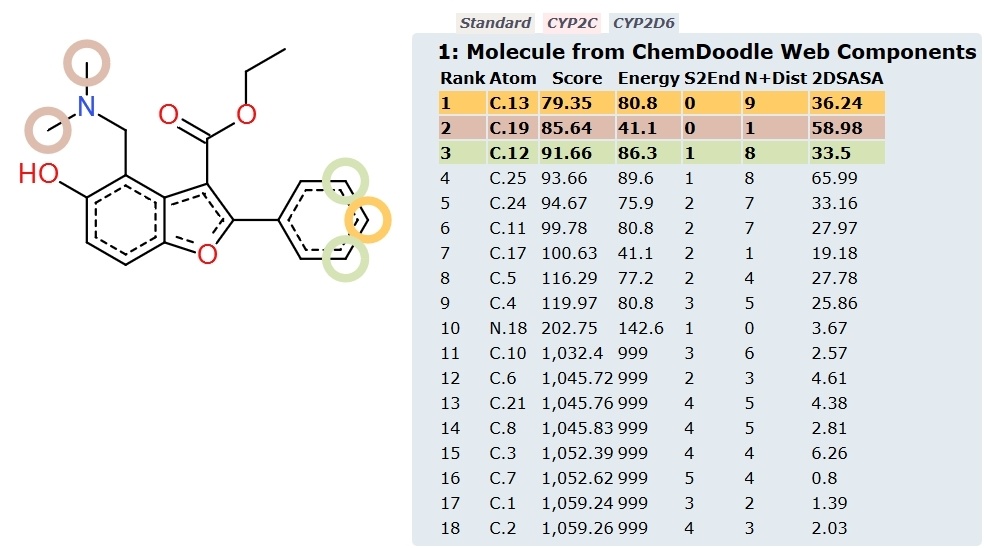
Три картинки получилось, потому что выданы предсказания интегральной стандартной опции и предсказания по 2 изоформам ферментов, участвующих в метаболизме 1 фазы: CYP 2C, CYP 2D6.
Думаю, вам интересно знать, по каким принципам работают подобного рода программы. Об одном из них, видимо, распространённом, вкратце можно почитать тут: http://crdd.osdd.net/raghava/metapred/algorithm.php.
А вот и краткая свежая сводная табличка: http://www.nature.com/nrd/journal/v14/n6/fig_tab/nrd4581_T2.html.
Спасибо за внимание. Продолжение следует.
Автор: superhimik






