Менее чем за неделю один твит Дэвида Синклера собрал 1 500 ретвитов, 5 200 лайков, что для его твиттера довольно много. Кто такой Дэвид Синклер? Это сейчас самый хайповый чувак в продлении жизни, профессор Гарварда, автор более 50 публикаций, опубликованных в рецензируемых журналах, в том числе в Nature, Cell и Science, организатор Национальной Академии Здоровья и Продолжительности Жизни, учредитель множество компаний, участник подкастов у Рогана и других шоу. Привлек уже как минимум 50 миллионов долларов. Дэвид недавно написал книгу “Продолжительность жизни”.

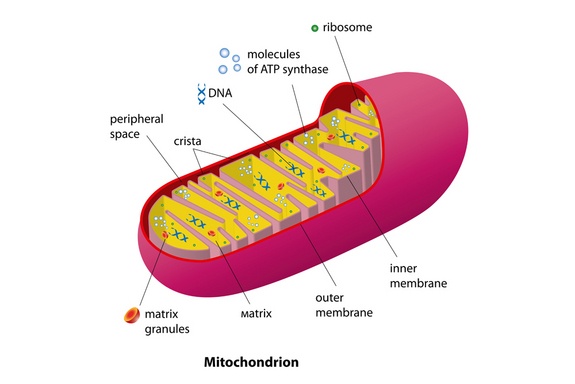
А еще он сооснователь Life Bioscience. Это такая семья компаний, нацеленных на продление жизни. Те, кто анализирует биотех компании, сразу обратят внимание на то, что на сайте этой компании нет раздела Pipeline — раздела, посвященному клиническим исследованиям. И нет раздела Science — где были б статьи. Не то, чтобы это прям совсем плохо, но просто отмечаем такую деталь. Правда, есть на этом сайте и хорошее: в фокусе компании обозначены несколько важных направлений — митохондрии, эпигенетика, воспаление и прочее. И дизайн симпатичный.

Дэвид Синклер.
А в твите он дал совет, как всем жить:
Читать полностью »