Как нам всем известно, иммунная система человека работает по принципу адаптации, порождая определенные антитела к определенным «вредителям» в крови. Анализ наличия/отсутствия тех или иных антител может рассказать о наличии/отсутствии тех или иных заболеваний у человека. Однако не всегда факт наличия антител можно приравнять к наличию болезни, поскольку важную роль играет и их количество. Современные методы количественного определения антител достаточно сложны и, честно признаться, дорогостоящи. Потому ученые из Американского химического общества (ACS) решили изобрести свою методику выявления и подсчета антител в крови за счет биолюминесцентных белков-датчиков и камеры смартфона. Какие именно физико-химические процессы задействованы в работе устройства, насколько точны его результаты, и как может измениться диагностика заболеваний благодаря этой разработке? Об этом мы узнаем из доклада ученых. Поехали.
Основа исследования
Антитела это белки плазмы крови, которые вырабатываются плазматическими клетками иммунной системы и уничтожают различные чужеродные вещества (бактерии, грибы, паразиты, вирусы и т.д.). Универсальных антител не бывает, каждые из них борются с чем-то определенным. Чужеродное вещество имеет свое «знамя» (антиген), которое оно гордо несет на поле боя. Распознав этот уникальный маркер, антитело атакует именно его. Эта война длится столько, сколько жизнь самого человека, в теле которого она протекает. Однако наша иммунная система не всегда способна справиться с врагом самостоятельно, тогда на помощь приходят лекарства и различные медицинские мероприятия. И, как мы знаем, первый и самый важный шаг в борьбе с болезнью это диагностика, т.е. реализация принципа «знай своего врага в лицо».
Как отмечают сами авторы исследования, в некоторых случаях диагностика по определению наличия тех или иных антител сводится к простому «да/нет», т.е. достойно знать, что антитела есть или их нет. Но вот в других ситуациях (как, например, в случае с нынешней пандемией) важную роль играет и количество антител.
Современные методы количественного анализа антител (иммуноферментный анализ, хемилюминесцентный иммуноанализ, поверхностный плазмонный резонанс, радиоиммунный анализ и т.д.) достаточно затратны, сложны и трудоемки.
Одним из самых важных критериев будущего устройства ученые называют его простоту, когда тест может выполнить любой неподготовленный человек в любых условиях, в том числе в районах с ограниченными ресурсами. Среди нынешних разработок в области миниатюризации средств анализа антител присутствуют и лаборатория на кристалле, и датчики нуклеиновых кислот, и датчики на базе оптоволокна. Все эти методы работают, однако они также требуют сложного оборудования, подготовленного персонала и довольно много времени. Не говоря уже о том, что большинство из них до сих пор реализуют принцип «да/нет», а не количественного определения.
Изменить столь неприглядную тенденцию в разработках могут сенсорные белки, основанные на биолюминесцентном резонансном переносе энергии (BRET от bioluminescence resonance energy transfer). Для POC тестирования* они хороши тем, что их сигналы можно обнаружить с помощью простых устройств, таких как камера смартфона.
POC тестирование* (point-of-care) — проведение медицинских тестов на месте пребывания пациента, т.е. без необходимости доставлять его биоматериал в лабораторию.
В качестве устройства, использующего преимущества BRET датчиков, ранее ученые предлагали микрофлюидное аналитическое устройство на бумажной основе (µPAD), в основе которого лежат BRET сенсорные датчики LUMABS (белки LUMinescent AntiBody Sensing).
Биолюминесцентный цвет LUMABS меняется с зеленого на синий в зависимости от концентрации целевого антитела, что позволяет количественно определять антитела в образцах крови с помощью цифровой камеры без какой-либо предварительной обработки образца или использования каких-либо реагентов.
Однако, несмотря на многие полезные особенности µPAD, их нелегко адаптировать к работе с очень малыми объемами крови (в диапазоне нескольких микролитров, мкл), прежде всего из-за технических ограничений процесса их уменьшения.
Например, вышеупомянутый µPAD основан на нескольких слоях бумаги, каждый из которых имеет значительный мертвый объем*. Следовательно, для надежного анализа требуется не менее 30 мкл цельной крови.
Мертвый объем* — объем вещества, которое остается в игле после инъекции (т.е. не участвует в тестировании). Данный термин часто применяется именно к образцам тестируемых веществ.
Кроме того, физический размер многослойного µPAD также предотвращает дальнейшее сокращение времени анализа (на данный момент нужно 20 минут), что затрудняет практическое применение POC тестирования.
Если же учесть, что забор крови через палец куда лучше подходит для POC тестирования, нежели венепункция, то объемы крови для тестирования будут ограничены. В среднем, объем крови, взятой из пальца взрослого человека, составляет около 10 мкл, а у ребенка (часто забор производится из пятки) около 5 мкл. Этот фактор также сильно влияет на формат будущего устройства и на принципы его работы.
Другой перспективной ветвью развития POC тестирования может быть
µTAD (microfluidic thread-based analytical devices) — аналитических устройств на основе микрожидкостных нитей. Разработка µTAD требует очень мало материалов, а результирующее устройство обладает довольно малыми габаритами и может работать с минимальным объемом образцов.
Ранее уже сообщалось об успешном проведении анализа крови с помощью µTAD, когда объем образца был не более 2 мкл, а время на сам тест составило пару минут. Однако µTAD методика пока еще нуждается в дополнительных этапах (применение рабочего буфера, субстрата, промывки) для получения результатов тестов. Другими словами, этот метод не совсем идеален, если говорить про портативное устройство диагностики, не требующее дополнительных ресурсов, устройств и навыков.
Потенциал µTAD, как говорят ученые, слишком велик, чтобы отметать эту технику, потому было решено ее немного усовершенствовать. В рассматриваемом нами сегодня труде ученые объединили µTAD и сенсорные BRET белки, что позволило создать устройство количественного тестирования антител посредством камеры смартфона. Стоит также отметить, что для анализа нужна всего лишь капля крови, а структура микро-нитей столь прочна, что можно проводить анализ сразу нескольких типов антител из этого объема.
Разработка устройства
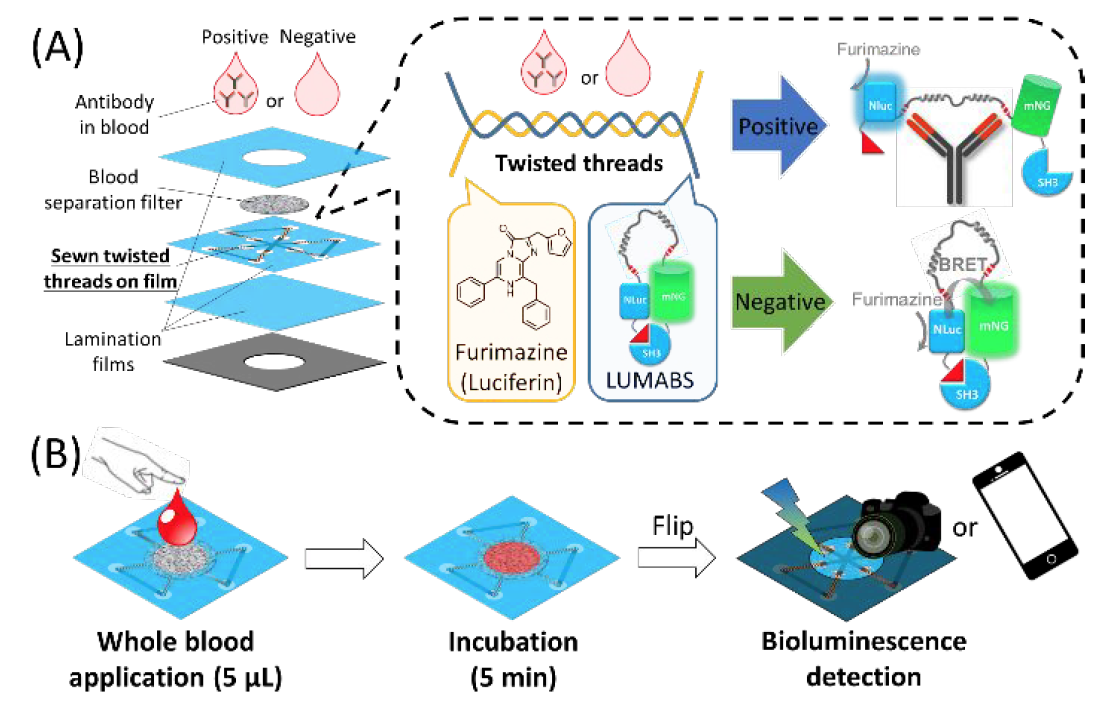
Изображение №1: А — схема механизма биолюминесцентной реакции µTAD, где LUMABS и его биолюминесцентный субстрат (фуримазин) были предварительно осаждены в сухом виде на две переплетенные хлопковые нити (цвет испускаемой биолюминесценции меняется с зеленого на синий в ответ на специфическое антитело). В — схема проведения теста: нанесение капли крови (5 мкл) на устройство и дальнейшее считывание биолюминесцентного сигнала цифровой камерой или камерой мобильного телефона спустя 5 минут инкубации.
Одним из важных условий для реализации тестера на основе BRET с полной интеграцией реагентов на устройстве является пространственное разделение люциферазы* и люциферина* для предотвращения их преждевременного смешивания и реакции.
Люциферазы* — окислительные ферменты, катализирующие реакцию биолюминесценции.
Люциферин — субстрат для люциферазы.
В ранее описанном µPAD устройстве сенсорный белок и субстрат люциферазы наносились на отдельные слои бумаги, что приводило к увеличению мертвого объема образца и продлению времени анализа. Подход µTAD позволяет использовать переплетенные нити, существенно увеличивая близость партнеров реакции.

Схема изготовления µTAD.
Хлопковая нить после кипячения (очистка) была разрезана на длину 60 см, потом вставлялась в иглу. На нить наносился гидрофобный слой (барьеры).
После поднятия и закрепления нити, чтобы она не касалась земли, 1.5 мкл раствора BSA в фосфатном буфере (8.1 мМ Na2HPO4, 1.47 мМ KH2PO4) с физраствором (137 мМ NaCl, 2.68 мМ KCl) и трегалозой (5 мас.%) наносили на участки нити, ограниченные вытянутыми гидрофобными барьерами.
После сушки в течение 15 минут (23-25 °C, 30-40% относительная влажность), 1.5 мкл каждого LUMABS в количестве, оптимизированном под определенную интенсивность сигнала (100 нМ для HIV-LUMABS, 100 нМ для HA-LUMABS или 25 нМ для DEN-LUMABS) в фосфатном буфере, содержащем 1 мг/мл BSA, наносили на срезы нитей, разделенные гидрофобными барьерами.
Далее следовало осаждение 15 мкл 20-кратно разведенного субстрата для анализа люциферазы (фуримазина) на противоположном конце нити. После еще одной сушки (15 минут) оба конца переплетались, чтобы LUMABS (люцифераза) и фуримазин (люциферин) находились в непосредственной близости. Скрученная нить вручную пришивалась на пластиковую пленку с предварительно сделанными отверстиями.
Мембрана для отделения крови помещалась поверх пластиковой пластины, прошитой нитями и зажатой между двумя слоями пленки (ламинирование) с вырезанным отверстием для ввода образца в верхнем слое.

Изображение №2
На 2А показано влияние числа переплетений нитей на устройство (HIV-LUMABS на область сигнала) после нанесения 5 мкл чистой пробы крови или пробы крови с добавлением анти-HIV (100 нМ).
При небольшом числе переплетений (особенно ниже 20) полученная интенсивность сигнала биолюминесценции была слишком слабой и неоднородной для получения значимых сигналов оттенка. Увеличение количества переплетений приводит к более воспроизводимым и однородным сигналам оттенка как для отрицательного, так и для положительного по антителам образца. Основываясь на этих результатах, было решено использовать 60 витков, что было оптимальным числом для воспроизводимого смешивания и реакции люциферазы и люциферина.
Использование гидрофобных барьеров позволяет наносить на одну нить сразу несколько LUMABS. Ввиду симметричного рисунка пришитой нити, модифицированной LUMABS и люциферином, получаются участки устройства, ориентированные по направлению к точке входа образца. Те же участки, которые имеют гидрофобные барьеры, оказываются расположенными в нижней части подложки из пластиковой пленки. Таким образом получается устройство с каждой областью обнаружения, нацеленной на разные аналита (объект анализа), обеспечивая равномерное распределение нанесенного образца крови.
Для сравнения было создано 4 варианта узора нитей (2В). Сравнение вариантов (a) и (b) показало, что оба гексагональных устройства позволяют обнаруживать 6 сигналов одновременно, но наблюдаемое среднеквадратическое отклонение для узора (b) в 2.7 раза больше, чем для узора (a). Это вызвано тем, что части секций нитей, излучающих биолюминесценцию, пересекаются участками, не излучающими свет, что приводит к неоднородному распределению люминесценции, поскольку сигналы собираются со дна устройств.
Среднеквадратическое отклонение, наблюдаемое на узоре (d), более чем в 2 раза выше по сравнению с (a) и ©. Скорее всего это вызвано сложностью узора, приводящей к увеличенному смещению гидрофильных и гидрофобных участков нитей.
Учитывая множество факторов (максимально доступное количество зон обнаружения сигнала, достижение однородности сигнала биолюминесценции и пригодность узора), именно вариант (а) был выбран в качестве оптимального узора для µTAD.
Результаты исследования
Изображение №3
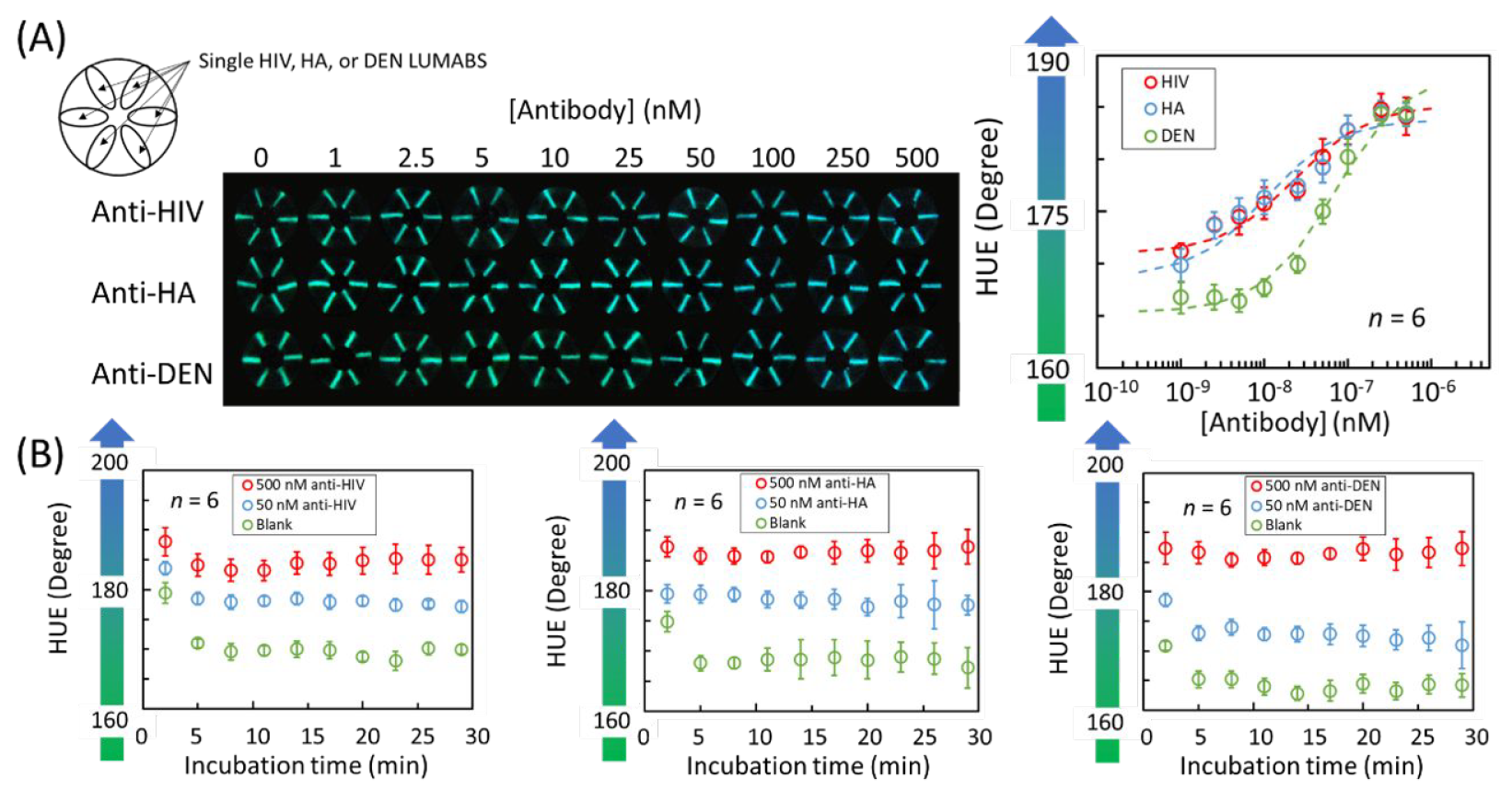
На 3А показаны данные считывания и кривые реакций для трех типов антител (по одному антителу на устройство) всего через 5 минут после внесения 5 мкл цельной крови вместе.
Из этих результатов видно, что среднеквадратическое отклонение не превышает 10%, как и планировалось, что указывает на равномерное распределение образцов по шести областям обнаружения сигналов.
Также было обнаружено, что сигналы оттенков, наблюдаемые при концентрациях 0, 50 и 500 нМ для трех модельных антител, были стабильными в течение 5-30 минут после нанесения образца (3В).
Пределы обнаружения (LOD), рассчитанные по методу 3-сигма, соответствовали 4.0 нМ для анти-HIV, 2.1 нМ для анти-HA и 14.9 нМ для анти-DEN.
HIV — вирус иммунодефицита человека; HA — гемагглютинин гриппа; DEN — вирус денге I типа.
Таким образом, использование µTAD, а не множества слоев бумаги в ранее описанном µPAD, и сближение люциферина и люциферазы за счет переплетения нитей позволили достичь не только стабильного сигнала биолюминесценции, но и уменьшения объема необходимой для теста крови.
Необходимо было также оценить, насколько будут эффективны следующие за прототипом устройства, т.е. не является ли прототип слишком сложным для повторного изготовления. Тесты с применением HIV-LUMABS показали, что относительное среднеквадратическое отклонение среднего значения c50 (концентрация антител, приводящая к 50% максимального изменения оттенка) составило 6.5% (c50 = 24.8 ± 1.6 нМ), что указывает на высокую воспроизводимость устройств при изготовлении.
Ученые отмечают, что для идеального POC тестера важную роль в эффективности анализа крови играет не только ее минимальный объем (объем образца), но и отсутствие зависимости от фактически примененного объема пробы в широком диапазоне. Ведь не всегда рассчитанные объемы соответствуют реальным.
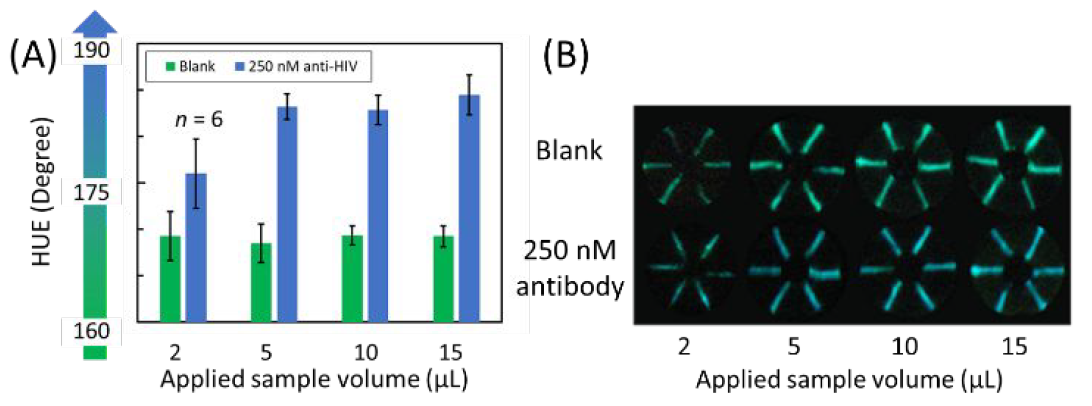
Изображение №4
На 4А и 4В показан биолюминесцентный ответ µTAD (все с HIV-LUMABS) через 5 минут после нанесения различных количеств (2-15 мкл) образцов цельной крови без/с HIV.
Анализ полученных данных показал, что при введении образца крови объемом 2 мкл смещение излучаемого биолюминесцентного цвета в ответ на целевое антитело было ниже, чем для больших объемов образца. В случае использования 5 мкл или выше полученный оттенок является постоянным независимо от примененного объема образца.
Причиной того, что 2 мкл недостаточно для успешного теста, является ограниченное смешивание люциферазы и люциферина, вызванное мертвым объемом. Это приводит к низкой интенсивности излучения биолюминесценции.
На следующем этапе была проведена оценка возможности µTAD определять сразу несколько разных антител. В этом тесте 5 мкл цельной крови с добавлением 500 нМ анти-HIV, 500 нМ анти-HA, 500 нМ анти-DEN или смеси всех трех вводили в µTAD.
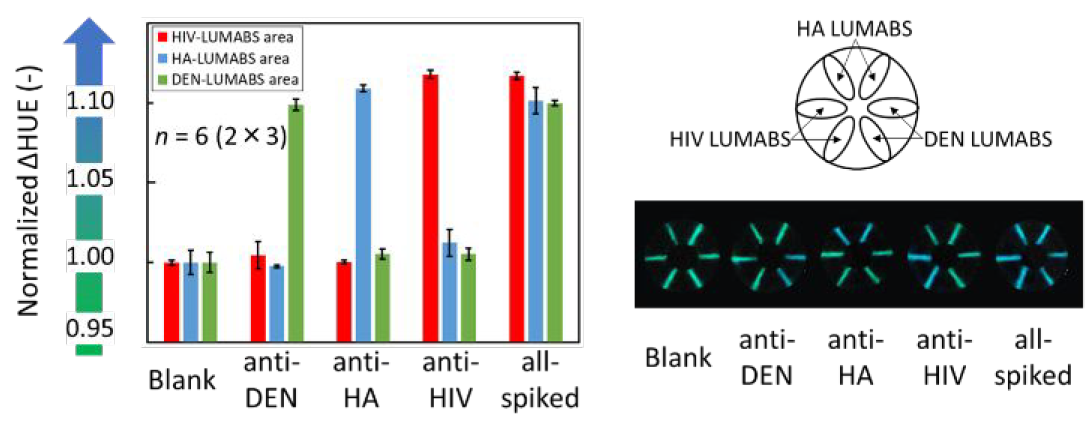
Изображение №5
В результате были получены селективные сигналы биолюминесценции, соответствующие каждому соответствующему антителу. Во-первых, это полностью доказывает, что можно успешно определять разные антитела одновременно. Во-вторых, это говорит о том, что узор, выбранный для µTAD, позволяет отдельным нитям не пересекаться, что нивелирует проблему перекрестных помех между биолюминесценцией, излучаемой из каждой области обнаружения. По прогнозам ученых их устройство способно распознавать до 6 разных антител одновременно.
Работоспособность устройства была успешно подтверждена вышеописанными тестами. Теперь необходимо было установить стабильность устройства спустя длительное время бездействия.
Для этого µTAD с HIV-LUMABS хранили в холодильнике (температура 4˚C, относительная влажность 23%) в вакуумной упаковке в течение 42 дней. Вакуумная упаковка нужна для предотвращения преждевременного окисления субстрата люциферазы (фуримазина).
Работоспособность хранимого устройства проверяли спустя разные интервалы времени с помощью холостого образца крови и образца с добавлением анти-HIV (250 нМ). Сравнение показателей устройства в первый день хранения и на 42-ой показало стабильные 95% первоначальной разницы в оттенках между анти-HIV-положительными и отрицательными образцами. Интенсивность биолюминесценции сохранялась примерно 90% от исходной в течение 30 дней.
Следовательно, µTAD сохраняют свою функциональность в течение месяца при надлежащем хранении в вакуумной упаковке и в холодильнике.
Рабочий µTAD излучает биолюминесцентный сигнал, который необходимо принять для его анализа. Роль приемника может сыграть как фотокамера, так и камера любого смартфона. Чтобы продемонстрировать эту функцию, сигналы биолюминесценции от µTAD, модифицированных HIV-LUMABS, регистрировались как цифровой камерой, так и камерой смартфона через 5 минут после нанесения 5 мкл образцов цельной крови с добавлением различных концентраций анти-HIV.

Изображение №6
На 3D-принтере был создан простой корпус (6С), защищающий образец от внешнего света. Этот маленький переходник также исключает необходимость в темном помещении для получения четкого биолюминесцентного сигнала. Таким образом, использование любого коммерчески доступного смартфона может позволить не только считывать сигналы µTAD устройств, но и послужить вычислительной платформой для их анализа. Однако этот аспект разработки пока не рассматривался.
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
Я не устану повторять, что диагностика в медицине играет очень важную роль в лечении того или иного заболевания. Зная, с чем мы боремся, мы может подобрать правильное лечение. Многие диагностические мероприятия требуют специальных устройств, подготовленного персонала, реагентов и, естественно, уйму времени, которого у пациента может и не быть.
В данном труде ученые продемонстрировали достаточно простое в изготовлении и использовании устройство, способное количественно определять антитела в крови. При этом требуется всего лишь 5 мкл крови для образца и 5 минут времени для получения конечного результата анализа. Роль анализатора играет система, совмещающая в себе µTAD (микроскопические хлопковые нити, покрытые специальным веществом) и BRET (система генерации биолюминесцентного сигнала в ответ на определенные антитела). А в качестве устройства приема сигналов может быть использована камера смартфона, что полностью нивелирует необходимость использовать сложное лабораторное оборудование и сопутствующих расходников.
Во многих местах нашей планеты нет супер-крутых лабораторий, как в сериале «Доктор Хаус», нет подкованных специалистов, нет возможности при малейшем сомнении сказать «сделайте пациенту МРТ и полный анализ крови на все-все-все». Всех этих благ в современной медицины нет, а вот болезни есть.
Авторы этой невероятной разработки считают, что знания, накопленные за многие годы исследований и технологического прогресса, уже сейчас позволяют нам создавать очень простые (и недорогие) устройства диагностики, которые можно использовать в любых условиях. Конечно, их детище пока не идеально, и множество усовершенствований еще будет сделано, но уже сейчас можно уверенно сказать, что подобная разработка спасет немало жизней.
Благодарю за внимание, оставайтесь любопытствующими и отличных всем выходных, ребята! :)
Немного рекламы
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Equinix Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Автор: Dmytro_Kikot