В посте об уязвимости к зависимостям я обещал написать о нейробиологической природе аддикций – то есть о том, что именно сейчас у нейроученых считается субстратом химической зависимости, будь то алкогольная, никотиновая, героиновая или какая-то другая зависома. Это одиннадцатая глава книги о зависимых гримасах бытия, пишу я ее уже третий год и однажды, надеюсь, допишу. Будут вопросы – отвечу.
Всем здоровья и свободы разной: внешней и внутренней.
1.
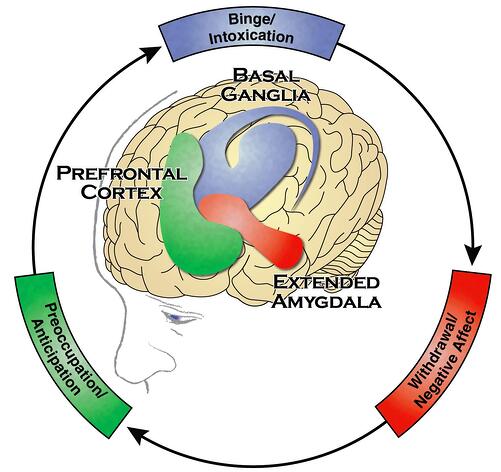
Если в нашем геноме затаились кое-какие проблемные гены, мы с большой вероятностью станем аддиктами, причем относительно рано, и зависимость наша будет протекать тяжело и беспросветно. А если гены в порядке? Это тоже ничего не гарантирует: воздействие достаточно высоких доз наделенных аддиктивным потенциалом веществ в течение длительного времени способно сделать нас зависимыми даже при «благополучном» геноме. Неважно, с каким набором карт мы вступаем в аддиктивную игру. Неважно, какое вещество мы вытянули из заманчиво блестящей кучи. И в том, и в другом случае мы запускаем нейроадаптивные процессы в определенных мозговых структурах. Эти процессы, при плохом раскладе, способны образовать так называемый аддиктивный цикл – нейробиологическую суть зависимости.
2.
человека состоит из 86 млрд нейронов, «общающихся» между собой электрическими сигналами через триллионы соединений. Эти соединения называются синапсами. Синапс состоит из пресинаптической и постсинаптической мембран. Пространство между мембранами называется синаптической щелью. Пресинаптическая мембрана при возбуждении нейрона выделяет специальные вещества – нейротрансмиттеры. Глутамат, ГАМК, дофамин, серотонин, норадреналин – это нейротрансмиттеры. Постсинаптическая мембрана имеет рецепторы к этим веществам. Когда молекула нейротрансмиттера взаимодействует с рецептором, нервный сигнал передается из одного нейрона другому. Главный нейротрансмиттер системы вознаграждения – дофамин.
Все аддиктивные вещества способны вызывать чувство удовольствия. Да, каждое из них вызывает еще и свои специфические эффекты. И, да, отношение между интенсивностью удовольствия и величиной аддиктивного потенциала нелинейно (другими словами, вещество, вызывающее наиболее интенсивное удовольствие, не обязательно должно занимать первое место в конкурсе аддиктивности). Но аддиктивным вещество делает именно его способность прямо или косвенно воздействовать на нейроны системы вознаграждения – фундаментального регулятора нашего поведения.
Вся наша поведенческая жизнь укладывается в формулу триггер – поведение – вознаграждение. Прилежащее ядро (лат. и англ. nucleus accumbens) – ключевое звено системы вознаграждения. Дорсальная область полосатого тела (лат. corpus striatum, pars dorsalis; англ. dorsal striatum) – ключевое звено в формировании привычек.
Вознаграждение мы переживаем как в форме предвкушения (желания, wanting), так и в форме удовольствия (liking). Wanting – форма мотивации, генерируемой обширными нейронными системами, частью которых является мезолимбическая дофаминовая система. Liking обусловлено активностью более мелких и хрупких нейронных систем и, похоже, зависит не столько от дофамина, сколько от энкефалинов. То, что в основе wanting и liking лежат разные механизмы, впервые предположили Кент Берридж и Терри Робинсон. Эта гипотеза была подтверждена и на лабораторных животных, и на людях. В прилежащем ядре примерно 90% wanting- и 10% liking-клеток. Остановитесь здесь и убедитесь, что поняли важность вышесказанного: хочу и нравится – это разные явления, причем разные они даже на уровне нейронов. Теперь смотрите, в чем именно важность: потребление ПАВ приводит к стимуляции только wanting-нейронов. Из-за этого wanting усиливается, тогда как liking не только не усиливается, но даже постепенно сходит на нет. Таким образом, можно сказать, что зависимость – это не проблема удовольствия, а проблема желания. Лимбическая сила, вон оно как! – скажете вы в сердцах. И будете правы. С годами голод по ПАВ все сильнее и сильнее, а удовольствия от употребления меньше и меньше – вот она, мякотка аддиктивной нейродрамы.
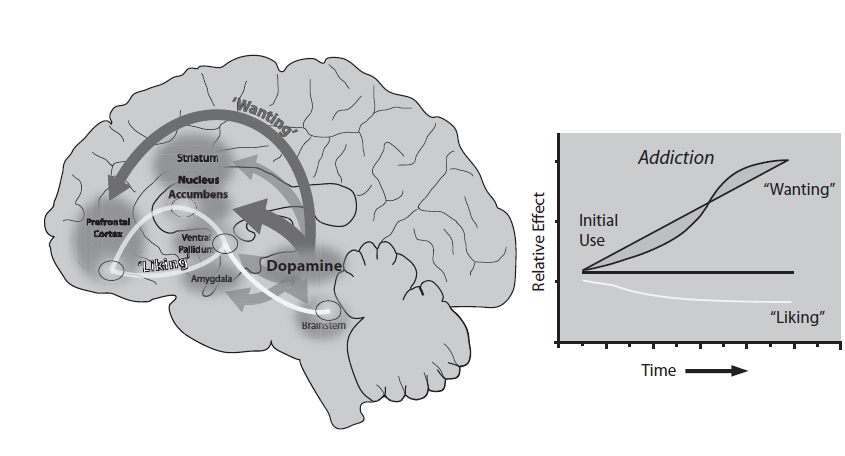
Теория Берриджа и Робинсона в целом сводится именно к этому: зависимое поведение возникает из-за функционального рассогласования между wanting- и liking-нейронами: по мере употребления ПАВ подопытные мыши (и люди) все больше want и все меньше like. И единственным способом унять wanting и повысить liking зависимые видят в продолжении употребления ПАВ, причем им приходится повышать дозу для получения желаемого уровня liking.
Дофаминовые системы не просто стимулируются, а сенситизируются. Сенситизация выражается в изменении морфологии нейронов, например, формы и количества дендритных шипиков (вспоминаем транскрипционные факторы NFκB и MEF2 из предыдущей главы). При этом wanting-нейроны становятся гиперреактивными к ПАВ и любым сигналам, сулящим получение ПАВ (drug cues): к рейнвейнской рюмке, запаху табачного дыма, музыке в стиле гоа-транс. В дальнейшем при воздержании от ПАВ сенситизированные нейроны не все время гиперактивны, конечно же. Но они могут становиться таковыми в триггерных ситуациях. Однажды вызванная, сенситизация очень длительна и, возможно, пожизненна.
Джордж Куб, директор NIAAA, и Нора Волкоу, директор NIDA, развили и дополнили концепцию Берриджа и Робинсона. В исследованиях, проведенных под их руководством, было показано, что чрезмерная активация нейронов nucleus accumbens приводит к нейроадаптивным изменениям как внутри системы вознаграждения, так и в других системах
Теперь о дорсальном стриатуме – главной структуре системы привычек (habit circuitry). В какой-то момент потребность в заветном веществе становится не просто сильной, а навязчивой, компульсивной: сам человек внутри себя может быть против употребления, но его будто никто не слушает – есть привычка, сильная и навязчивая, и ее нужно день за днем поддерживать. Не хочу, а уже надо, и это надо будто живет своей собственной жизнью. Причем навязчивое надо продолжается даже после перехода в трезвость. Абстиненты много месяцев подряд замечают у себя смутную, временами усиливающуюся потребность что-то делать и «зацикливаются» на том или ином поведении: часами играют в видеоигры, запойно погружаются в сериалы, с головой уходят в спорт, не совсем понимая, что следуют компульсивному зову, примерно такому же, который управлял их поведением во времена употребления ПАВ.
Итак, в основе сильного, непреодолимого влечения к ПАВ лежит сенситизация (морфофункциональные изменения) дофаминовых нейронов прилежащего ядра. При этом уровень удовольствия (liking) не только не растет, но даже снижается. Параллельно с этим в дело вовлекаются нейроны дорсального стриатума, прочно встраивая поиск и употребление ПАВ в габитуальный план жизни.
3.
Помимо прилежащего ядра и полосатого тела, в какой-то момент на аддиктивную сцену выходит амигдала (лат. corpus amygdaloideum, англ. amygdala). Это парная миндалевидная структура – по одной штуке в каждой височной доле. Амигдала играет ключевую роль в формировании эмоций (в частности, страха), запоминании эмоционально окрашенных событий и принятии решений. Как видно, амигдала – один из топ-менеджеров нашего поведения.
Нейроны амигдалы содержат большое количество рецепторов к кортикотропин-рилизинг-фактору (КРФ), норадреналину, динорфинам – нейротрансмиттерам стресс-систем
Норадреналин обеспечивает поведенческий ответ во время стресса, возбуждая нейроны и фокусируя внимание на стрессоры. КРФ и норадреналин активируют друг друга.
Динорфины – пептиды, тропные к κ-опиоидным рецепторам. Динорфины опосредуют негативные эмоциональные состояния, в том числе аверсию, дисфорию и депрессию. А еще динорфины повышают порог вознаграждения и угнетают высвобождение дофамина. Так же как и КРФ, активность динорфинов повышается при отмене ПАВ у лиц с аддикцией.
В принципе, здесь мы можем остановиться и задуматься вот над чем. Почему люди чаще всего пьют? «Хочу выпить сто грамм для аппетита». Хорошо. Еще? «Ну, вся компания пьет, и поэтому...» Ладно, еще? «Я устал, весь день у меня копился стресс, шеф вывел из себя, жена бесит, спина болит...» – есть такое? Ирония вот в чем: несмотря на то, что в краткосрочной перспективе ПАВ действительно могут снять напряжение, в то же время они активируют нейротрансмиссию КРФ, норадреналина и динорфинов. Это приводит к тому, что эмоциональное состояние зависимых ухудшается по нарастающему – у кого-то быстро и явно, у кого-то медленно и еле заметно. Алкоголь, героин, никотин и другие ПАВ не снимают стресс, а усиливают его, так как повышают уровень КРФ, норадреналина и динорфинов.
Лучше всего это показано в 5-минутном мультике Nuggets: идет по ровной поверхности птица киви, видит каплю, идет дальше. Видит еще одну каплю, пробует на вкус. И вдруг все вокруг становится солнечно-желтым, появляется чарующая музыка, киви взлетает и какое-то время порхает с блаженным видом. Потом эффект капли проходит, птица приземляется и шагает дальше. Время от времени ей встречаются такие же капли. Киви их выпивает. Желтый цвет, музыка, полет. Но с каждым разом полет более кратковременный, падения более жесткие, а окружение – вот это важно – становится все более темным и мрачным. Именно так выглядит мир для человека с чрезмерно активными стресс-системами амигдалы: мир для него серый и чуждый, многое навевает грусть, пугает или раздражает. Несчастной птице остается только одно: найти еще одну капельку, чтобы хоть на короткое время вернуть эфемерный желтый свет, не понимая, что мир так почернел именно из-за этих капель и что после каждой капли он станет еще чернее.
Очевидно, если продолжать употреблять ПАВ, изменения в стресс-системах амигдалы с годами будут только усиливаться. А если прекратить? Если убрать все ПАВ, пережить синдром отмены – дальше будет нормально? К счастью, да. Но не сразу. Есть такой термин: protracted abstinence. По-русски: подострая абстиненция. Люди, которые 10, 15, 20 лет увлеченно алкоголизируются, а потом перестают пить, не так быстро возвращаются в комфортное эмоциональное состояние – сенсибилизированной амигдале для восстановления нужны месяцы, а порой даже годы.
(Стоит добавить, что гиперактивация амигдалы возможна и при других состояниях, например, при посттравматическом стрессе или хронической боли. У таких людей аддиктивная уязвимость выше, а восстановление требует большего времени.)
4.
Что может быть хуже, чем негативное эмоциональное состояние из-за взъерошенной, потрепанной амигдалы? Самое неприятное, что я сам вынес из своего 15-летнего аддиктивного опыта, это быть неразумным в своих же глазах. Я не мог смириться с тем, что курю, но и не мог бросить. Дискомфорт, который мы испытываем, когда наше поведение не вяжется с нашими убеждениями, Леон Фестингер назвал когнитивным диссонансом. Правда, диссонанс исчезал в момент, когда я, проснувшись утром, делал заветную первую затяжку. Все знают о кошке Шредингера. Мою душу то царапала, то не царапала кошка Фестингера.
Под воздействием ПАВ дофаминовая трансмиссия подавляется не только в системе вознаграждения, но и в префронтальной коре. Из-за этого ухудшаются исполнительные функции: саморегуляция, принятие решений, гибкость в выборе и инициировании действий, присвоении значимости и контроль ошибок. Далее нейропластические изменения затрагивают и глутаматергическую передачу. Нарушенная трансмиссия дофамина и глутамата в префронтальных областях
5.
Все, что происходит с нейронами базальных ганглий, амигдалы, префронтальной коры вследствие употребления ПАВ, находит отражение в желаниях, эмоциях, мыслях человека, на решения, которые он принимает, на поведение и жизнь. Что именно с нейронами происходит? Мы теперь знаем, что: усиливается экспрессия разных транскрипционных факторов, активируются гены, синтезируются белки, нервная клетка претерпевает морфологические и функциональные изменения, сенситизируясь к определенным сигналам. Эти изменения называются нейропластическими.
Нейропластичность – суть научения. Наш
А вот по ответу на этот вопрос пока нет научного консенсуса. Да, мы можем найти диагноз «синдром зависимости» среди расстройств психики и поведения в Международной классификации болезней 10-го пересмотра. Мы можем найти клинические рекомендации по лечению зависимости. И заключить: раз этот диагноз попал в МКБ-10 и раз это лечат лекарствами, то это болезнь. По некоторым формальным признакам зависимость можно рассматривать как расстройство, я с этим согласен. А вот нейробиолог Марк Льюис не согласен. Свое несогласие он вынес в подзаголовок книги «Биология желания», он так и звучит: «Зависимость не болезнь». Дискуссия о природе зависимости меня захватила сильно, и я, похоже, буду писать отдельную книгу про это. Здесь лишь кратко отмечу вот что. Марк Льюис утверждает, что все, что лежит в основе аддикции, укладывается в понятие научения (learning):
Здесь я хочу закончить словами Кента Берриджа: «Может быть, это и весело: спорить о словах, о том, какие из них лучше всего описывают зависимость. Но, я думаю, споры о словах, например о том, следует ли говорить «болезнь мозга», а не о реальных особенностях и механизмах самой зависимости, легко могут стать ловушками и отвлечь нас от более важных целей. Эти цели должны состоять в том, чтобы определить основные черты и механизмы зависимости и подумать о лучших способах помочь зависимым».
Пока ученые между собой договариваются, мы можем извлечь из их дискуссии нечто, с чем согласны все стороны: в основе зависимости лежит научение нейронов и нейронных цепей. И сделать три практических вывода: 1) пока человек продолжает употреблять ПАВ, изменения, лежащие в основе зависимости, будут прогрессировать; 2) если перестать употреблять, эти процессы остановятся; 3)
Автор: Marat Aghinyan




